Bệnh mang Amip (AGD): Hướng dẫn thực tế - phần 1

Trong phần đầu tiên của một đánh giá hai phần về bệnh mang Amip (AGD), John Angles khám phá lịch sử về mầm bệnh, đã nổi lên để trở thành một trong những thách thức sức khỏe toàn cầu quan trọng nhất mà các nhà sản xuất cá hồi phải đối mặt trong thập kỷ qua.
Tàu thủy thường được sử dụng cho điều trị AGD
Những thách thức về môi trường và sinh học hiện diện trong mọi doanh nghiệp nuôi trồng thủy sản và nuôi cá hồi Đại Tây Dương cũng không ngoại lệ, với con cái nhiễm bệnh từ các loài Caligus và Lepeophtheirus salmonis, cũng như nhiều bệnh mang khác nhau bao gồm bệnh giun tròn tăng sinh hay mang Amip (AGD) trở thành những thách thức lớn nhất. Nếu không được kiểm soát hoặc điều trị, AGD có thể dẫn đến tăng trưởng chậm, lười ăn và thường tử vong phổ biến. Trọng tâm của bài viết này là để hiểu rõ hơn các yếu tố liên quan đến AGD và mối quan hệ giữa mầm bệnh, vật chủ và môi trường, trong khi phần thứ hai sẽ xem xét tình trạng nghiên cứu hiện tại.
Lịch sử
AGD lần đầu tiên được xác định là ảnh hưởng đến cá hồi Đại Tây Dương nuôi tại Tasmania vào năm 1984, và từ đó trở thành một bệnh dịch đặc hữu thường xuyên xảy ra ở đó, đặc biệt là trong cá hồi chưa được nuôi. Vì vậy, nhiều nông dân nuôi cá hồi ở Tasmania đã điều chỉnh chiến lược sản xuất của họ để điều trị AGD ngày càng tăng một cách thường xuyên trong suốt giai đoạn với việc sử dụng các phương pháp thả tắm nước ngọt (FW), được quản lý trong tàu thủy hoặc bạt.
Mặc dù hydrogen peroxide (H₂O₂) đã được sử dụng như một phương pháp điều trị, nhưng rất nguy hiểm cho cá nếu sử dụng quá lâu hoặc ở nhiệt độ cao, gây ra căng thẳng oxy hóa đáng kể. Tắm FW trong 3-4 giờ biểu hiện thành công hơn nhiều, mặc dù tiếp cận với số lượng đầy đủ của FW cho điều trị bằng tàu thủy hoặc bạt thì nó vẫn là một vấn đề đối với một số địa điểm. Cho dù phương pháp nào được sử dụng, nó cũng sẽ tăng thêm chi phí đáng kể cho sản xuất, thông thường từ 10 đến 20 phần trăm.
Ireland lần đầu tiên ghi nhận trường hợp AGD vào cuối mùa thu năm 1995, Scotland năm 2006 và Na Uy vào cuối mùa thu năm 2006 tại bốn địa điểm khác biệt về mặt địa lý. Ở Na Uy, các cuộc kiểm tra mô bệnh học cho thấy amip đồng thời trong các tổn thương phù hợp với sự bùng phát của AGD, mặc dù nó không gây ra các vấn đề nghiêm trọng cho đến năm 2013.
Kinh nghiệm của Ireland và Scotland đối với căn bệnh này tương tự nhau, với các trường hợp nghiêm trọng được ghi nhận từ năm 2011. Ireland, Scotland và Na Uy đều bị ảnh hưởng bởi sự bùng phát của AGD ngay sau khi giới thiệu cả cá hồi non S0 và S1 ra biển để phát triển; cá tự nhiên có xu hướng nhạy cảm hơn.
Phương pháp điều trị được sử dụng để được chỉ định tùy thuộc vào lấy mẫu thường xuyên của mang cho các dấu hiệu tổng trên tất cả tám vòm mang (16 hemibranchs) và sau đó so sánh bằng cách sử dụng một trang trại làm cơ sở đánh giá. Tuy nhiên, kể từ năm 2009, các dấu hiệu gộp đã được so sánh trực quan với một biểu đồ điểm được phát triển và mô tả bởi Taylor với số điểm bằng 0 cho thấy mang khỏe mạnh và điểm 5 biểu thị chất nhầy và tổn thương rộng lớn bao phủ hầu hết bề mặt mang (Bảng 1).
Bảng 1. Nhiễm trùng, điểm số mang, mô tả tổng
| Cấp độ nhiễm trùng | Điểm mang | Tổng mô tả |
| Rõ ràng | 0 | Không có dấu hiệu nhiễm trùng và màu sắc lành mạnh |
| Rất nhạt | 1 | 1 đốm trắng, sẹo ánh sáng hoặc vệt hoại tử không xác định |
| Nhạt | 2 | 2-3 đốm / miếng nhầy nhỏ |
| Vừa phải | 3 | Kèm theo vết nhầy dày hoặc các nhóm đốm lên đến 20% diện tích mang |
| Nâng cao | 4 | Các tổn thương bao gồm tới 50% diện tích mang |
| Nghiêm trọng | 5 | Các tổn thương rộng khắp bao gồm hầu hết bề mặt mang |
Khi AGD lần đầu tiên hiện diện ở Tasmania vào năm 1984, các quan sát tổng thể, bệnh lý lâm sàng và mô bệnh học (nghiên cứu thay đổi mô do bệnh) đã xác định hai amip đơn bào sống tự do, Neoparamoeba pernaquidensis và Neoparamoeba branchiphila là các tác nhân gây bệnh. Tuy nhiên, sự trình tự gen mô bệnh học bằng cách sử dụng các xét nghiệm phản ứng chuỗi polymerase (PCR) của amip không mang tính nuôi cấy (NCGD) cho thấy rằng cả hai đều không liên quan đến tổn thương AGD.

Điểm số AGD mang lại, từ 0 (trên cùng bên trái) đến 5 (dưới cùng bên phải) © Mark Adams và Hamish Roger
Thay vào đó, một trùng Amip NCGD mới được phát hiện vào năm 2007, người Nuraramoeba perurans, và điều này sớm được biết đến như là nguyên nhân có khả năng xảy ra. Một amip sinh thái biển, N. perurans là ký sinh trùng sống tự do, và dễ dàng gắn vào mang cá hồi và sau đó nhân lên nhanh chóng nhờ sự phân chia tế bào đơn giản. Nhiễm trùng gây tăng sản và kết hợp của biểu mô tế bào và hình thành u nang hoặc túi nang.
Mô bệnh học chỉ ra rằng các khối mỏng này liên kết lại với nhau và làm giảm đáng kể diện tích bề mặt chức năng của mang, tùy thuộc vào mức độ kết hợp của hạt mỏng. Sự suy giảm chức năng mang này có thể dẫn đến tình trạng thiếu oxy, nhiễm toan và cuối cùng là tử vong.
Các yếu tố tạo điều kiện gắn kết bao gồm những thay đổi trong môi trường vật chủ, chẳng hạn như tăng độ mặn và nhiệt độ; các tác nhân sinh học như vi khuẩn, tảo, động vật nguyên sinh hoặc sứa; và các yếu tố vật chủ khác có thể có mặt và đóng góp. Do đó, người ta cho rằng có một số nguyên nhân tạo thuận lợi cho sự lây lan của AGD. Tuy nhiên, theo Tiến sĩ Hamish Rodger, giám đốc quản lý toàn cầu của Fish Vet Group, trong khi những yếu tố này có thể góp phần cho AGD, việc phơi nhiễm cá đối với N. perurans đơn phương mà không có sự thỏa hiệp cũng sẽ dẫn đến sự lây lan nhanh chóng của AGD.
Biến động độ mặn của nước biển (SW) và giá trị pH thực chất liên quan đến nhiệt độ bề mặt SW. Mặc dù không kết luận, nhiệt độ SW cao hơn được cho là sẽ hỗ trợ sự gia tăng của N. perurans, dẫn đến bùng phát AGD. Bằng chứng gần đây cho thấy rằng mức độ mặn lớn hơn 32 phần nghìn (ppt) đóng một vai trò quan trọng không kém trong sự khởi đầu của AGD, có thể là do sự có mặt của rất nhiều Song chiên tảo (Tảo đơn bào 2 roi ) và tảo cát, các loại sinh vật phù du với nước có độ mặn và có thể làm tổn hại đến mang. Nếu độ mặn giảm xuống dưới 28 ppt thì bệnh lâm sàng sẽ không xuất hiện. AGD tăng sinh ở nhiệt độ 10 ° C đến 16 ° C; nhiệt độ tối ưu để nuôi cá hồi Đại Tây Dương là 6 ° C đến 16 ° C.
Tại Na Uy, đợt bùng phát đầu tiên theo nhiệt độ SW đạt 3,5 ° C trên mức bình thường trong thời gian đó trong năm, và trong hầu hết các đợt bùng phát khác, nhiệt độ SW trước khi nhiễm cao hơn mức trung bình theo mùa. Tuy nhiên, dịch bệnh AGD đã xảy ra ở Scotland ở nhiệt độ thấp tới 7,5 ° C, chỉ ra rằng nhiệt độ đơn độc không phải là nguyên nhân vấn đề. Nhưng nhiệt độ cao hơn sẽ cho phép AGD phát triển nhanh hơn và có tác động đáng kể hơn.
Các nghiên cứu gần đây cho thấy cá hồi có thể phát triển tính kháng sau nhiễm trùng đầu tiên. Tuy nhiên, từ giai thoại kinh nghiệm, nếu điều trị đầu tiên được thực hiện khi điểm số mang ở mức 1,5 đến 2 hoặc cao hơn thì nhiễm trùng liên tục (và do đó điều trị) gần như không thể tránh khỏi. Ở phía Tây Nam Ireland trong giai đoạn 2011-2013, tôi đã làm việc trên một đi quản lý chín phương pháp điều trị tắm FW cho cùng một con cá trong giai đoạn phát triển, với tỷ lệ tử vong tích lũy lớn hơn 50%).
Có thể lập luận rằng S1s của 80-100g chuyển sang biển trong tháng tư có thể tăng nguy cơ kháng AGD nếu chúng được điều trị trong phòng tắm FW lên đến ba giờ ngay sau khi bệnh lý tổng phát hiện điểm số 1 đến 1,5. Lưu ý rằng các hồ chứa chính cho bệnh vẫn là cá hồi nuôi, bắt buộc phân chia các cấp bậc tuổi được đề cử ở các vịnh có nhiều hơn một trang trại và các giai đoạn thích hợp sau đây xảy ra để giảm tần suất điều trị.
Điều trị sớm là hết sức quan trọng, trước khi điểm số của mang đạt đến 1 và ngay sau khi kết quả dương tính PCR mô bệnh học xuất hiện. Một ấn phẩm gần đây của Downes và cộng sự cho thấy rằng các xét nghiệm chẩn đoán phân tử không phá hủy thời gian thực sử dụng mẫu tăm bông mang (trái ngược với mẫu lấy mỡ) có thể phát hiện sự có mặt của N. perurans trong vòng 48 giờ đầu tiên và sau đó tại mỗi mẫu . Đây là một phát triển quan trọng trong phát hiện sớm.
Abdon Ryan, giám đốc chăn nuôi cho Marine Harvest Ireland South West cho thấy N. perurans hiện diện trong môi trường biển quanh năm và, theo thỏa thuận với Tiến sĩ Rodger, cho rằng sự xuất hiện theo mùa của nhiều vi sinh vật khác nhau có thể thỏa hiệp mang và tạo điều kiện cho N. perurans đeo bám và nhân thêm. Abdon nói thêm rằng mức cao nhất của tổn thất sản xuất ở Ireland xảy ra trong giai đoạn 2011-2013, với tỷ lệ tử vong đáng kể ở các trang trại ở phía Bắc và Nam.
Trong thời gian gần đây, tỷ lệ tử vong do AGD đã giảm đáng kể - chủ yếu là do hiểu biết tốt hơn về bệnh và các phương pháp chăn nuôi tốt hơn. Gần đây, một địa điểm ở phía Tây Nam Ireland đã giới thiệu S1s vào tháng 4 và ngay sau khi bệnh lý tổng thể chỉ ra điểm số từ 1 đến 1,5 vào tháng 6, bồn tắm FW được thực hiện trên toàn bộ điểm nuôi, với tỉ lệ tử vong thấp. Các phương pháp điều trị khác được tiến hành vào tháng 8 và tháng 10, một lần nữa với tỷ lệ tử vong thấp và không cần phải điều trị thêm cho đến khi thu hoạch. Điểm nuôi này đã trải qua 90% sự sống còn trong giai đoạn phát triển do điều trị sớm và hiệu quả.
Từ những kinh nghiệm trước đây trong năm 2011, nếu điều trị đầu tiên không được thực hiện khi điểm số thấp (dưới 1), thì các phương pháp điều trị tiếp theo sẽ chỉ nhằm giảm tác động đáng kể của AGD và các tổn thất đáng kể có thể xảy ra. Các phương pháp điều trị dự phòng hoặc phòng ngừa cũng đã được thử nhưng có ít hoặc không có lợi ích.
Rất nhiều nghiên cứu đã được thực hiện trên các bệnh mang và AGD trong thời gian gần đây trong nỗ lực làm sáng tỏ nguyên nhân. Điều này đã dẫn đến nhiều nhà bình luận sử dụng thuật ngữ “bệnh mang phức tạp” thay vì AGD vì nhiều tác nhân gây bệnh, kể cả amip, có thể góp phần gây bệnh.
Hamish Rodger báo cáo rằng nghiên cứu hiện tại đang có xu hướng tập trung vào các mầm bệnh mang như:
a) Epitheliocystis, một tình trạng ảnh hưởng đến mang nhiều cá thể và cá biển bao gồm cá hồi, do vi khuẩn gram âm gây ra. Loại vi khuẩn chủ yếu được cho là Candidatus Branchiomonas cysticola Ca. B. cisticola) đã được tìm thấy và lây truyền ở cả cá hồi khỏe mạnh và cá hồi mang bệnh và có liên quan đến bệnh lý mang.
b) Vi rút Pox là một vấn đề lớn trong cá FW nhưng hiện đã được phát hiện trong cá biển. Siêu vi khuẩn mang mầm bệnh cá hồi (SGPV) có thể làm giảm khả năng miễn dịch bẩm sinh, tạo thuận lợi cho cuộc xâm lược của những kẻ xâm lược thứ cấp như AGD. Apoptosis là một biểu thị của SGPV đang hiện diện.
c) Ký sinh trùng microsporidian của chấy và cá hồi gọi là Desmozoon lepeophtherii có thể góp phần gây bệnh nhưng vẫn chưa được xác nhận.
Có thể bạn quan tâm
Phần mềm

Phối trộn thức ăn chăn nuôi
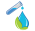
Pha dung dịch thủy canh

Định mức cho tôm ăn

Phối trộn phân bón NPK

Xác định tỷ lệ tôm sống

Chuyển đổi đơn vị phân bón

Xác định công suất sục khí

Chuyển đổi đơn vị tôm

Tính diện tích nhà kính

Tính thể tích ao hồ



 Lãi cao từ nuôi cá trắm, chép giòn
Lãi cao từ nuôi cá trắm, chép giòn  Vai trò của sốc đối với bệnh Cá
Vai trò của sốc đối với bệnh Cá